"ما هي مشتقات مركب الفوران؟
ما هي التأثيرات السلبية لمركب الفوران ومشتقاته؟
كيف تمّ تصنيع مشتقات الفوران؟
ما هي مشتقات مركب الفوران؟
الفيورانات، بما في ذلك الفوران، 2-ميثيل فوران، 3-ميثيل فوران، و2،5-ثنائي ميثيل فوران هي مركبات منخفضة الوزن الجزيئي يمكن تحليلها بسبب تقلبها العالي؛ وذلك إما عن طريق استخراج فراغ الرأس الثابت أو فراغ الرأس / الاستخراج الدقيق للطور الصلب باستخدام كروماتوجرافيا الغاز المقترنة بالكتلة قياس الطيف.
أثناء تحضير عينة الفوران، يلزم أخذ درجات الحرارة المنخفضة (حوالي +4 درجات مئوية) في الاعتبار بعناية لتجنب الخسائر المحتملة ومع ذلك، هناك حاجة إلى درجات حرارة أعلى (تصل إلى 50 درجة مئوية) أثناء حضانة العينة لتعزيز إطلاق الفيوران في فراغ الرأس، ويتم تحقيق تأثير مماثل عن طريق إضافة الملح، لا ينصح بدرجات حرارة حضانة عالية (تتجاوز 60 درجة مئوية)، حيث يمكن تكوين فيوران إضافي ويعتمد القياس الكمي للفيوران على الإضافات القياسية أو المعايرة الخارجية، بما في ذلك الديوتيريوم المعياري.
احتجزت الفيورانات جذور الأريل، الناتجة عن أكسدة أحماض أريل بورونيك ومن أريلهيدرازينات بواسطة Mn (OAc) 3، لإعطاء مشتقات (2-arylfuran)، حيث بدأ شق بيرفلورو ألكيل الذي تم إنتاجه باستخدام ديثيونيت الصوديوم في إضعاف مشتقات الفيوران عبر إضافة إلى موضع الفيوران 2 ، كما يتم إضافة شق إيثوكسي كاربونيل ميثيل، الناتج من زونثات 51 بواسطة بيروكسيد ديالورويل إلى موضع 5 من 2-أسيتيل فوران، ممّا يعطي منتج الإضافة.
ما هي التأثيرات السلبية لمركب الفوران ومشتقاته؟
الديوكسينات والفيوران، وهما من الملوثات البيئية المعروفة، شديدة السمية للإنسان والعديد من الأنواع الأخرى. يتم إطلاق ثنائي بنزوفيوران في الهواء من مصادر الاحتراق، ويتم إدراجه كملوثات مثيرة للقلق بسبب ثباته في البيئة وإمكانية التراكم الأحيائي، والسمية للإنسان والبيئة، حيث تكون هذه المركبات عند امتصاصها في التربة أو الركائز الأخرى، شديدة الثبات في ظل الظروف البيئية العادية.
من بين ما يزيد عن 200 من أيزومرات ثنائي بنزوديوكسين ودايبنزوفيوران متعدد الكلور، لا تعتبر جميعها سامة على قدم المساواة ولا تعتبر قوية مثل المواد المسرطنة، استنادًا إلى مفهوم وكالة حماية البيئة الأمريكية (EPA) للعوامل المكافئة السامة (TEFs) لتقييم مخاطر الإصابة بالسرطان المرتبطة بهذه المواد الكيميائية، (يعتبر TCDD) الأكثر فاعلية، حيث ترتبط فعالية السرطان لجميع الأيزومرات الأخرى المكلورة في 2،3،7 ، و8 مواضع بـ TCDD و(tetrachlorodibenzofuran) (TCDF).
من الضروري معرفة نسبة إجمالي الديوكسينات والفيورانات عند حساب المعادلات السامة. اعتمادًا على الجرعة وطول فترة التعرض لهذه المركبات، قد تتطور حالات صحية مختلفة، مثل السعال والتهابات الجهاز التنفسي الحادة والتهاب الشعب الهوائية المزمن وآلام البطن وآلام العضلات وحب الشباب وتغيرات في لون الجلد والصداع وزيادة الدهون الثلاثية في الدم، والقيء والإسهال وكثرة الكريات البيض وألم الأطراف العصبية والاعتلال العصبي المحيطي وتنمل وفقدان الوزن وأمراض الكبد، كما أنّها مسؤولة عن التسبب في مرض “يوشو” (تشمل الأعراض الشائعة الآفات الجلدية والعينية، وعدم انتظام الدورة الشهرية وانخفاض الاستجابة المناعية وفي الأطفال، كانت هناك تقارير عن ضعف النمو المعرفي).
كيف تمّ تصنيع مشتقات الفوران؟
تم تصنيع الفيوران الذي يحتوي على (fulgides 33 و38) ثم اشتقاقه لاحقًا ودورانه تحت ظروف كيميائية ضوئية لتزويد المواد بخصائص ضوئية إذ يتفاعل الفولجيدات (33 مع malononitrile) و (diethylamine) في (THF) لتوفير مشتق (dicyanomethylene 35)، والذي خضع لدورة كيميائية ضوئية في التولوين المركب عند 366 نانومتر لتوفير الفوتوكرومات 36، خضعت هذه الفوتوكرومات الزرقاء المستقرة حرارياً للتفاعل العكسي عند التعرض للضوء الأبيض وأعطت (Z -fulgides 38) مركبات ثنائي سيانوميثيلين المقابلة 39 تحت ظروف تفاعل مماثلة. في التولوين، تمت إيزومرة 39 أولاً إلى (E) -40 قبل أن يخضع للدورة عند 366 نانومتر لتوفير المشتق ثلاثي الحلقات.
تم تصنيع سلسلة من الأوكسازولات المستبدلة بالفوريل وخصائصها الطيفية والإنارة مقارنة بمركبات فينيل وثيوفينيل المماثلة وقد تم العثور على نظائرها المحتوية على الفوران على حد سواء تمتص الضوء وتنبعث منه بأطوال موجية أطول من نظائرها 2،3-ديفينيلوكسازول، ولكن بأطوال موجية أقصر من نظائرها من الثيوفين، يُرجح أن يرجع الاتجاه الملحوظ إلى الاستقطاب الأكبر لحلقة ثيوفين على حلقة الفوران والفينيل.
أدى دمج مجموعات الكربونيل في حلقة الفوران إلى نفس التحول تقريبًا إلى أطوال موجية طويلة في أطياف الامتصاص كما في نظير 2،3-ديفينيلوكسازول وثيوفين، بالنظر إلى التحول من 20 إلى 40 نانومتر، فإنّه لا يرجع فقط إلى الاقتران الممتد الذي يوفره الكاربونيل، ولكن أيضًا إلى طبيعة قبول الإلكترون للمجموعة، يشير اختلاف أطياف الامتصاص في التولوين والإيثانول إلى أن الجزيئات قطبية بشكل ضعيف في الحالة الأرضية، ويتم حلها بشكل أفضل بواسطة التولوين، ولكن عند الإثارة يتم تحويل كثافة الإلكترون إلى مجموعة الكربونيل، ممّا يزيد من استقطاب الأنواع ويسمح للحالة المثارة بأن تكون أفضل إذابة في الإيثانول القطبي المذيب 46-51.
"
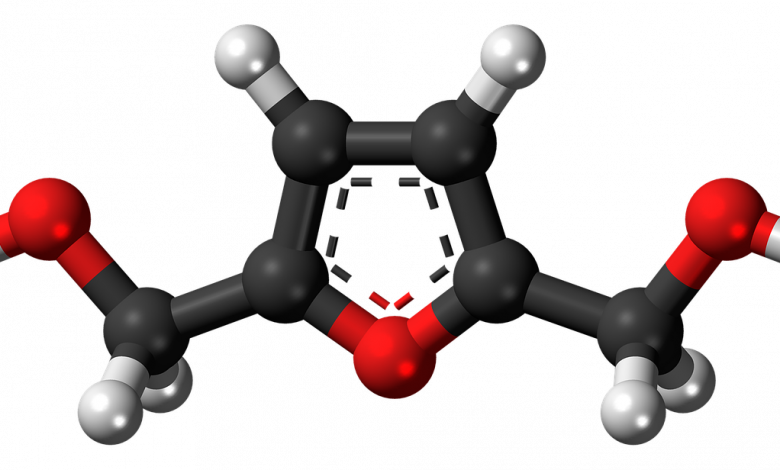
مشتقات مركب الفوران
هل أعجبك هذا المقال؟
