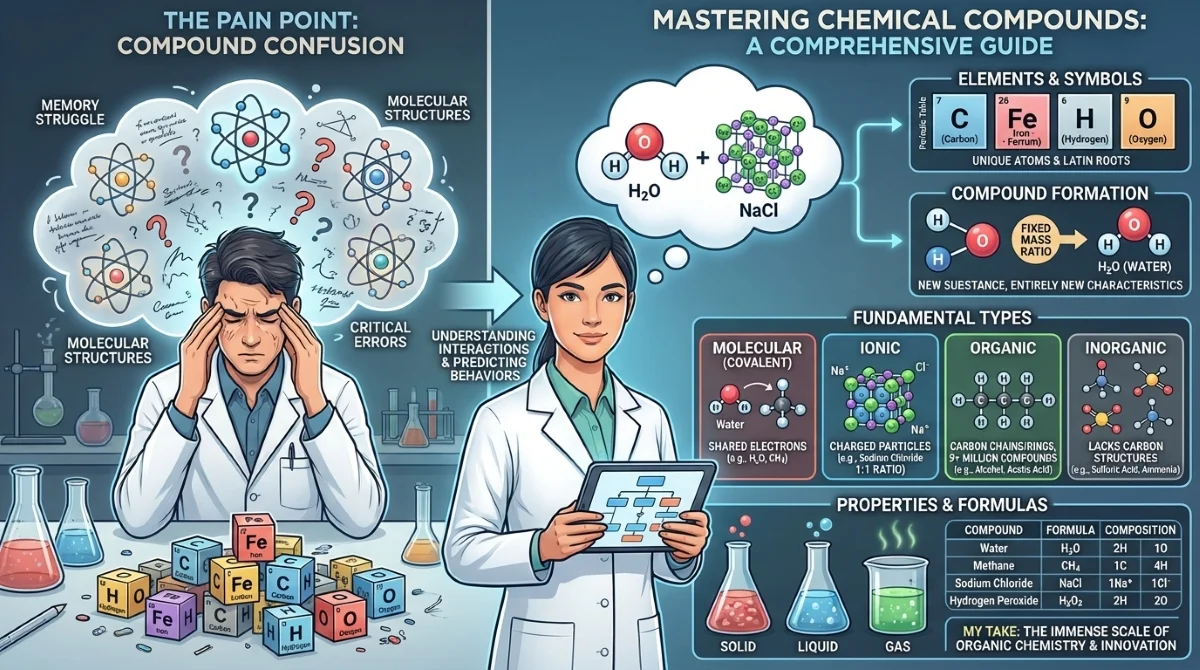
إتقان فهم المركبات الكيميائية يمثل غالباً نقطة ألم رئيسية لطلاب العلوم وفنيي المختبرات الذين يكافحون لحفظ الهياكل الجزيئية. يحلل هذا الدليل الشامل التعريفات الدقيقة والأنواع والخصائص الخاصة بالمركبات الكيميائية لمساعدة المتعلمين على تحديد الروابط الجزيئية والأيونية بثقة. ومن خلال فهم كيفية تفاعل الذرات، يمكن للقراء التنبؤ بدقة بالسلوكيات الكيميائية وتجنب الأخطاء الفادحة في البيئات الأكاديمية أو المهنية.
يتكون الكون من ذرات تعود لأكثر من 100 عنصر كيميائي مختلف، ويتميز كل عنصر بخصائص فريدة. على سبيل المثال، تختلف البنية الذرية لعنصر الكربون تماماً عن عنصر الحديد أو عنصر الذهب. يتم تحديد كل عنصر برمز فريد يتكون من حرف واحد أو حرفين أو ثلاثة أحرف، وغالباً ما يُشتق من اسمه اللاتيني الأصلي، مثل رمز Fe لعنصر الحديد (ferrum)، أو ببساطة رمز C، ورمز H، ورمز O لعناصر الكربون والهيدروجين والأكسجين على التوالي. عندما تتحد هذه العناصر كيميائياً بنسبة كتلية ثابتة، فإنها تشكل مركباً جديداً، وتفقد خصائصها الفردية الأصلية تماماً لتكوين مادة ذات خصائص جديدة كلياً.
الأنواع الأساسية للمركبات الكيميائية
تُصنف المركبات على نطاق واسع إلى أربعة أنواع رئيسية: المركبات الجزيئية (أو التساهمية)، والمركبات الأيونية، والمركبات العضوية، والمركبات غير العضوية. تتكون المركبات الجزيئية، مثل الماء ومركب الميثان، من جزيئات متميزة تتشكل عبر مشاركة الإلكترونات. وعلى العكس من ذلك، تعتمد المركبات الأيونية على الجسيمات المشحونة للحفاظ على بنيتها.
على سبيل المثال، لا يحتوي كلوريد الصوديوم على جزيئات فعلية من مركب NaCl؛ بل يتكون من أعداد متساوية من أيونات الصوديوم الموجبة الشحنة (Na+) وأيونات الكلوريد سالبة الشحنة (Cl-) بنسبة صارمة تبلغ 1:1. علاوة على ذلك، تُعرف المركبات العضوية باحتوائها على سلاسل أو حلقات من ذرات الكربون، وقد تم عزلها في الأصل من الكائنات الحية.
ونظراً لأن الكربون يمكن أن يرتبط بنفسه وبعناصر أخرى بطرق متنوعة للغاية، فقد حدد العلماء أكثر من 9 ملايين مركب عضوي مختلف. وأي مادة تفتقر إلى هذه الهياكل الكربونية المحددة تندرج تحت فئة المركبات غير العضوية.
الخصائص الفيزيائية والصيغ الكيميائية
تُظهر المركبات الكيميائية مجموعة محيرة من الخصائص الفيزيائية في ظل درجات الحرارة والضغوط العادية. فهي توجد على شكل مواد صلبة، أو سوائل، أو غازات، وتعرض كل الألوان عبر الطيف المرئي. يعتبر التوازن الهيكلي دقيقاً للغاية؛ حيث يمكن أن يؤدي استبدال ذرة واحدة فقط داخل المركب إلى تغيير لونه، أو رائحته، أو سميته بشكل جذري، مما يحول مادة أساسية للحياة إلى خطر مميت.
ولتتبع هذه الهياكل بدقة، يستخدم العلماء الصيغ الكيميائية كتمثيل رمزي لنسب الذرات. على سبيل المثال، الصيغة الكيميائية لمركب الميثان هي CH4، مما يشير إلى نسبة دقيقة تتكون من ذرة كربون واحدة إلى 4 ذرات من الهيدروجين. يوضح الجدول التالي المركبات والصيغ المحددة المذكورة صراحة في البيانات الكيميائية التأسيسية:
| اسم المركب | الصيغة الكيميائية | التكوين الذري |
|---|---|---|
| الماء | H2O | ذرتان هيدروجين، وذرة أكسجين |
| الميثان | CH4 | ذرة كربون، و 4 ذرات هيدروجين |
| كلوريد الصوديوم (ملح الطعام) | NaCl | أيون صوديوم (Na+)، وأيون كلوريد (Cl-) |
| بيروكسيد الهيدروجين | H2O2 | ذرتان هيدروجين، وذرتان أكسجين |
| الكحول | C2H6O | كربون، وهيدروجين، وأكسجين |
| حمض الخليك | C2H4O2 | كربون، وهيدروجين، وأكسجين |
| حمض الكبريتيك | H2SO4 | هيدروجين، وكبريت، وأكسجين |
| الأمونيا | NH3 | نيتروجين، وهيدروجين |
| أكسيد النيتروز | N2O | نيتروجين، وأكسجين |
رؤية تحليلية: النطاق الهائل للكيمياء العضوية
يسلط الحجم الهائل للتركيبات الكيميائية الضوء على التعقيد اللامتناهي للعلوم الجزيئية. إن الحقيقة الصريحة بوجود أكثر من 9 ملايين مركب عضوي لمجرد أن الكربون يمكنه الارتباط بشكل متنوع مع نفسه ومع العناصر الأخرى، تمثل مقياساً مذهلاً. يثبت هذا النطاق الهائل أن الكيمياء العضوية ليست مجرد موضوع أكاديمي ثابت، بل هي حدود تتوسع باستمرار للابتكار الصيدلاني والصناعي.
علاوة على ذلك، فإن فهم التمييز بين الهياكل الجزيئية والشبكات الأيونية، مثل تركيبة أيون Na+ وأيون Cl- في كلوريد الصوديوم، يعد أمراً أساسياً لعلوم المواد. وعندما يدرك الطلاب والباحثون أن المركب المتشكل حديثاً يفقد بشكل دائم خصائص عناصره الأساسية، فإنهم يطلقون العنان للقدرة على هندسة مواد تركيبية جديدة تماماً. في النهاية، يعد إتقان هذه الصيغ التأسيسية المتطلب الأساسي المطلق لأي اكتشاف علمي متقدم.