محتويات المقال
الزئبق: خصائصه، استخداماته، وحقيقة أنواعه (الأحمر، الأبيض، والأسود)
يُعد الزئبق (Mercury) عنصراً كيميائياً فريداً يحمل الرمز Hg وعدده الذري 80. يتميز بأنه المعدن الوحيد الذي يوجد في الحالة السائلة عند درجات الحرارة والضغط القياسيين، مما يجعله يتخذ شكل حبيبات خرزية مستديرة بسبب توتره السطحي العالي. لا يوجد الزئبق حراً في الطبيعة عادةً، بل يرتبط بعناصر أخرى مكوناً مركبات كيميائية أشهرها "كبريتيد الزئبق".
مصادر الزئبق في الطبيعة
يتواجد الزئبق في القشرة الأرضية بكميات ضيلة، ويتم الحصول عليه بشكل رئيسي من خام "السينابار" (Cinnabar) أو الزنجفر، وهو معدن لين يتراوح لونه بين الأحمر والبني، ويتم استخلاص الزئبق النقي منه عبر عمليات التعدين والتسخين.
كما ينطلق الزئبق في البيئة نتيجة عوامل طبيعية وبشرية، منها:
-
البراكين والفيضانات وعوامل التعرية.
-
حرق الفحم الحجري والمخلفات في محطات توليد الطاقة.
-
صناعة الإسمنت.
الخصائص الفيزيائية والكيميائية
ينتمي الزئبق إلى مجموعة المعادن الانتقالية، ويتمتع بخصائص مميزة منها:
-
الحالة الفيزيائية: سائل فضي اللون، يتحول إلى لون مائل للأزرق عند التجمد.
-
الخصائص الكهربائية والمغناطيسية: موصل جيد للكهرباء ويمتلك قدرة عالية على تكوين مجالات مغناطيسية، كما يمتاز بمقاومية كهربائية عالية.
-
التفاعلات: لا يتأثر بالهواء العادي، لكنه يتفاعل مع الأوزون والهلجينات (مثل الكلور) في درجة حرارة الغرفة.
-
الإذابة: يُعد مذيباً جيداً للعديد من المعادن كالذهب والفضة والصوديوم (مكوناً ما يعرف بالملغم)، لكنه لا يذيب الحديد.
-
الخصائص الأخرى: يتميز بضغط بخاري مرتفع، لزوجة منخفضة، وقوة تماسك ذرية ضعيفة، وهو سريع التبخر والانتشار.
استخدامات الزئبق الشائعة
يدخل الزئبق في العديد من التطبيقات الصناعية والعلمية، أبرزها:
-
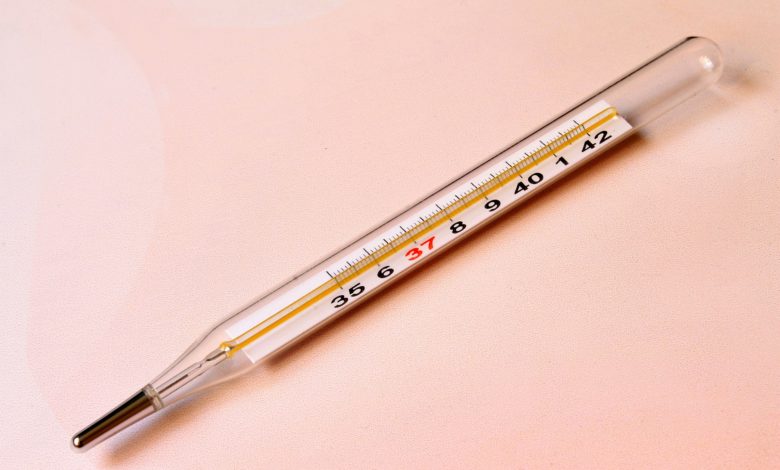
الأجهزة العلمية: مثل موازين الحرارة (الترموستات) والباروميترات (مقاييس الضغط).
-
الإضاءة: يستخدم في مصابيح الشوارع ومصابيح الفلورسنت.
-
التعدين: له دور محوري في استخلاص الذهب من خاماته.
-
الطب: يدخل في صناعة حشوات الأسنان (الأملغم).
-
الصناعات الكيميائية: يستخدم في إنتاج هيدروكسيد الصوديوم والكلور عبر التحليل الكهربائي.
-
البطاريات: يدخل في تصنيع بعض أنواع البطاريات الجافة.
أنواع الزئبق (بين العلم والاستخدامات الخاصة)
تتعدد المسميات المرتبطة بالزئبق بناءً على تركيبه واستخداماته، ومنها:
-
الزئبق الأبيض:
هو الشكل الأكثر شيوعاً واستخداماً في موازين الحرارة الطبية والصناعية. يتميز بتمدده السريع بالحرارة وانكماشه بالبرودة. يتواجد أحياناً في الصخور الناتجة عن البراكين أو الشهب، وقد يتغير لونه تدريجياً عند التعرض المستمر للشمس. -
الزئبق الأحمر:
مادة مثيرة للجدل، توصف غالباً بأنها مواد عضوية وأنسجة حيوية أو مشتقات معالجة بالإشعاع. تشير بعض المصادر إلى استخدامه في تطبيقات عسكرية متقدمة مثل القنابل الاندماجية (كمفجر بدائي) أو في تخصيب اليورانيوم، مما يجعله مادة خاضعة لرقابة صارمة لمنع انتشار أسلحة الدمار الشامل. كما ارتبط تاريخياً بخرافات التحنيط في العصور القديمة. -
الزئبق الأسود:
يوصف بأنه مادة ذات كثافة عالية جداً (أعلى من اليورانيوم) وباهظة الثمن. ارتبط قديماً بالأساطير واستخدامات المشعوذين، بينما تشير أبحاث حديثة إلى إمكانية استخدامه في تطبيقات نووية دقيقة نظراً لخصائصه الفيزيائية الفريدة.
المخاطر الصحية والبيئية
يُصنف الزئبق كعنصر سام وخطير جداً. يمكن أن يدخل جسم الإنسان عبر الاستنشاق، البلع، أو حتى من خلال الجروح المفتوحة. يؤدي التراكم الحيوي للزئبق إلى:
-
تلف في الجهاز العصبي، الكبد، والكلى.
-
أعراض التسمم: تهيج الرئتين، الغثيان، ارتفاع ضغط الدم، طفح جلدي، وشعور بالخدر في الأطراف.
-
التأثير البيئي: يلوث المسطحات المائية ويتبخر لينتشر في الجو، مما يضر بالكائنات البحرية والسلسلة الغذائية.
أبرز مركبات الزئبق
-
أكسيد الزئبق: مسحوق أحمر ينتج عن تسخين الزئبق في الهواء، ويتفكك بالحرارة ليعطي الأكسجين والزئبق.
-
كلوريد الزئبق (السليماني): ينتج عن إذابة أكسيد الزئبق في حمض الهيدروكلوريك المركز.
-
كلوريد الزئبق (الكالوميل): مركب أبيض شحيح الذوبان في الماء، يستخدم في تطبيقات طبية وكيميائية محددة.
-
أسيتات الزئبق: مركب عضوي شديد السمية يستخدم في التحضيرات الكيميائية العضوية.
إرشادات السلامة والتخزين
للتعامل الآمن مع منتجات الزئبق، يجب اتباع التالي:
-
تخزينه في عبوات "غير قابلة للكسر" ومحكمة الإغلاق.
-
وضع ملصقات تحذيرية واضحة تبين محتوى العبوة وسميتها.
-
حفظه بعيداً تماماً عن متناول الأطفال.
-
يفضل تخزينه بالقرب من مواد ماصة للزيوت أو السوائل لاحتواء أي تسرب محتمل.
-
في حال الرغبة بالتخلص منه، يجب اللجوء إلى الجهات المختصة بإدارة النفايات الخطرة وعدم رميه في القمامة المنزلية أو الصرف الصحي.